Les pesticides sont-ils responsables de la maladie de Parkinson ? La recherche s'accélère avec les résultats de plusieurs études récentes qui mettent en cause des molécules très utilisées en France et au Canada.Le point sur un dossier qui continue de poser une énigme.
Des millions de personnes prennent des médicaments pour faire baisser leur taux de cholestérol dans l'espoir d'éviter un infarctus. Le Dr Michel de Lorgeril, en deux livres parfaitement documentés – le dernier paraissant ces jours-ci - a montré que c'est à peu près aussi efficace que la croix Vitafor que l'on pendait à son cou dans les années 1960. La différence, c'est que la croix Vitafor, si elle n'apportait pas « joie, bonheur, santé et chance » comme le promettaient les annonces dans France Dimanche ou Télé Poche ne mettait pas non plus la vie des crédules en danger. Avec les médicaments anticholestérol, c’est une autre histoire. Le corps médical découvre aujourd’hui que ces médicaments peuvent augmenter le risque de cancer.
Au contraire des médias français, restés étonnamment silencieux, la presse américaine commente ainsi depuis plusieurs jours les résultats calamiteux de l’étude SEAS, rendus publiques le 2 septembre 2008. L’étude portait sur 1873 patients ; 105 de ceux qui prenaient un médicament contre le cholestérol (en France, Inegy) ont développé un cancer, contre 70 de ceux qui prenaient un placebo. Le Dr Terje Pedersen de l’Hôpital universitaire de Ulleval en Suède est l’auteur principal de cette étude financée par deux laboratoires américains. Pressé de questions par les journalistes américains, il a soutenu que cette association est « probablement due au hasard ». Raisons invoquées : on ne disposerait pas d'un mécanisme pouvant expliquer cette association et rien ne permettait jusqu’ici d’associer médicaments anticholestérol et cancers. Il s’agit là d’un gros mensonge.
D’abord, on sait depuis 1996 que tous les médicaments du cholestérol présents à l’époque sur le marché provoquent des cancers chez l’animal. Mais chez l’homme aussi, il y avait des raisons d’être prudents.
En 1970, l'Organisation mondiale de la santé (OMS) a mis sur pied une étude de prévention cardiovasculaire auprès de 10 627 hommes : une partie prendrait du clofibrate, un médicament contre le cholestérol élevé, l'autre un placebo. Par rapport au placebo, le clofibrate augmenta la mortalité cardiovasculaire (208 décès, contre 173 dans le groupe placebo) et surtout la mortalité par cancers. En dépit de ces états de service calamiteux, le clofibrate devait obtenir une autorisation de mise sur le marché en France au début des années 1970, et n'en être retiré qu'en… 1990. [1]
De 1973 à 1983, un autre médicament anticholestérol, la cholestyramine, fit l'objet d'une étude contre placebo, baptisée Lipid Research Clinics Coronary Primary Prevention, auprès de 3 800 personnes présentant un cholestérol très élevé. Sept ans plus tard, par rapport au placebo, la cholestyramine avait réduit le cholestérol de 6,7% et la mortalité cardiovasculaire de 1,7% seulement. En 1992, on dénombrait plus de cancers gastro-intestinaux et de cancers du pharynx dans le groupe traité. Mais cet excès ne fut pas considéré significatif sur le plan statistique.[2]
En 1982, le laboratoire américain Parke-Davis lança le gemfibrozil (Lipur), autre merveille contre le cholestérol,qui fut aussitôt inclus dans une étude clinique conduite pendant 5 ans à Helsinki auprès de 4 081 hommes présentant un " mauvais " cholestérol (LDL) élevé. Par rapport au placebo, le gemfibrozil entraîna une diminution modeste des accidents coronariens. Mais la prise du médicament n'eut aucun effet sur la mortalité totale. Les chercheurs poursuivirent l'essai trois ans et demi dans l'espoir de faire enfin apparaître un bénéfice net. Hélas, s'ils décomptèrent 83 morts dans le groupe qui avait reçu le placebo, ils en relevèrent 18 de plus dans celui qui avait pris le médicament - une différence due à un excès de cancers. Dix huit mois plus tard, dans un étonnant rectificatif, ils décidèrent de reclasser 13 des décès du groupe placebo dans la rubrique " cancers ", avant de conclure que l'augmentation des cancers et de la mortalité dans le groupe traité par gemfibrozil était " probablement due au hasard. " Enfin, dans un article de synthèse ultérieur rédigé à l'intention des prescripteurs, ils ne firent plus mention de la mortalité totale.
- Dans l’étude CARE de 1996, il y a eu plus de cancers du sein chez les femmes qui prenaient une statine (la pravastatine) que chez celles qui prenaient le placebo : 12 cas de cancers (pour 291 femmes traitées) contre un seul cas (toujours pour 291 femmes traitées) [3][4]
- Dans l’étude PROSPER, publiée en 2002, il y a eu 25% de nouveaux cas de cancer en plus chez les patients qui avaient pris le médicament anticholestérol (pravastatine - Elisor) par rapport à ceux qi prenaient le placebo. Interrogés à ce sujet, les auteurs de l’étude payée par Bristol-Myers Squib ont répondu à l’époque que ce résultat « ne les inquiétait pas particulièrement (sic) » dans la mesure où il concernait plusieurs types de tissus et que « les cancers étaient probablement déjà là avant le traitement. »[5]
D’autres études n’ont pas trouvé que les personnes soignées avec des médicaments anticholestérol ont eu plus de cancers. [6] L’étude HPS est à ce jour la plus importante à avoir testé une statine (simvastatine - Lodales). Pendant 3 ans, 10 000 volontaires ont pris une statine. Il n’y a pas eu plus de cancers dans le groupe qui prenait le médicament que dans le groupe qui prenait le placebo.
Comment expliquer que dans certains cas le traitement anticholestérol ne semble pas augmenter le risque de cancer, et que dans d’autres cas il en soit à l’origine ?
Pour commencer, on n’est pas sûr que les cas de cancer, s’il y en a eu, ont bien été rapportés. En 2003, le British Medical Journal a calculé que sur 164 essais cliniques portant sur les statines, seuls 48 avaient rapporté le nombre de participants affectés par des effets indésirables. [7]
En 2007, une équipe de chercheurs de l’université Tufts de Boston a fait une découverte troublante en analysant les résultats de 23 études sur les statines : plus le « mauvais » cholestérol LDL diminue, plus on voit le risque de nouveaux cas de cancer augmenter (voir figure ). [8]
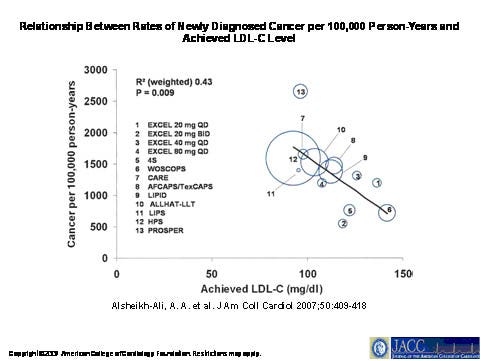
En 1998, des chercheurs hollandais avaient trouvé, en suivant près de 40 000 hommes et femmes, que le taux de cholestérol est inversement associé au risque de cancer : plus le cholestérol est bas, plus le risque de cancer est élevé : +54% chez les hommes, +30% chez les femmes. [9]
Il est donc possible qu’un cholestérol trop bas, et en particulier un cholestérol-LDL trop bas (celui que les médecins veulent faire baisser) expose à un risque accru en dévoilant des cancers latents. A cet égard, les risques des médicaments du cholestérol et peut-être même des aliments anticholestérol (pâtes à tartiner et autres) l’emportent probablement sur les bénéfices.
Références :
[1] Report of the Committee of Principal Investigators. WHO cooperative trial on primary prevention of ischaemic heart disease with clofibrate to lower serum cholesterol: final mortality follow-up. Lancet 1984;2:600 -4
[2] The Lipid Research Clinics Coronary Primary Prevention Trial. Results of 6 years of post-trial follow-up. The Lipid Research Clinics Investigators.
Arch Intern Med. 1992 Jul;152(7):1399-410.
[3] Sacks FM, Pfeffer MA, Moye LA, Rouleau JL, Rutherford JD, Cole TG, et al. The effect of pravastatin on coronary events after myocardial infarction in patients with average cholesterol levels. N Engl J Med 1996;335:1001–9.
[4] Lewis SJ et al. Effect of pravastatin on cardiovascular events in women after myocardial infarction: The Cholesterol and Recurrent Events (CARE) trial. J Am Coll Cardiol 1998 Jul 32 140-146.
[5] Shepherd J, Blauw GJ, Murphy MB, et al, on behalf of the PROSPER study group. Pravastatin in elderly individuals at risk of vascular disease (PROSPER): a randomized controlled trial. Lancet. 2002;360:1623-1630.
[6] Cauley JA, McTiernan A, Rodabough RJ, LaCroix A, Bauer DC, Margolis KL,
Paskett ED, Vitolins MZ, Furberg CD, Chlebowski RT; Women's Health Initiative
Research Group. Statin use and breast cancer: prospective results from the Women's Health Initiative. J Natl Cancer Inst. 2006 May 17;98(10):700-7.
[7] Law, M.R. et al. Quantifying effect of statins on low-density lipoprotein cholesterol, ischaemic heart disease, and stroke: systematic review and meta-analysis. BMJ. 2003 June 28; 326 (7404): 1423.
[8] Alsheikh-Ali AA, Maddukuri PV, Han H, Karas RH. Effect of the magnitude of lipid lowering on risk of elevated liver enzymes, rhabdomyolysis, and cancer: insights from large randomized statin trials. J Am Coll Cardiol. 2007 Jul 31;50(5):409-18.
[9] Knekt P, Reunanen A, Aromaa A et al. Serum cholesterol and risk of cancer in a cohort of 39 000 men and women. J Clin Epidemiol. 1998;41:519-530.






